Anfang April fiel bei GE Pharmaceuticals der Startschuss für reguläre Herstellung von fälschungssicheren Pharmaverpackungen mit Seriennummer. Im Auftrag des Pilotkunden Wörwag Pharma produzierte der österreichisch-bulgarische Dienstleister GE Anfang April 2016 die ersten Chargen für den europäischen Markt. Damit gehören die Partner Wörwag und GE zu den ersten Unternehmen in Europa, die serialisierte Verpackungen in Kombination mit einem Tamper Evidence-Verschluss herstellen – gemäß der ab 2019 geltenden EU-Richtlinie 2011/62/EU.
Drei Jahre vor Ablauf der Übergangsfrist setzen sie damit den technischen Maßstab in Europa. Ab dem 9. Februar 2019 verpflichtet die als „Falsified Medicines Directive“ (FMD) bekannte EU-Richtlinie sämtliche Pharmaproduzenten, serialisierte und fälschungssichere Verpackungen zu produzieren. „Mit Wörwag haben wir nun einen ersten Anwender, der erfolgreich in die FMD-konforme Serienproduktion eingestiegen ist“, betont Dr. Günter Datz, Geschäftsführer der GE Pharmaceuticals Ltd. „Dank unserer ausgereiften technischen Lösung können wir ab sofort allen interessierten Pharmaherstellern die FMD-konforme Produktion ihrer Sekundärverpackungen anbieten.“ Der Verpackungsspezialist GE betreibt in seinem neu errichteten Werk in Botevgrad bei Sofia sechs Produktionslinien und baut die Kapazitäten weiter aus. Zwei Linien sind bereits auf die FMD-konforme Produktion ausgerichtet, weitere FMD-Linien sind im Aufbau.
Im Vorgriff auf die FMD-Richtlinie begann die GE Pharmaceuticals zusammen mit Wörwag frühzeitig, die Produktion neu auszurichten. Von Beginn an mit dabei waren deutsche Dienstleister wie der Maschinenbau-Spezialist Baumer Hhs und der Faltschachtellieferant Kroha. Unter Federführung des deutsch-bulgarischen Managementduos von GE, Dr. Günter Datz und Angel Angelov, entwickelte das Projektteam ein neues Verpackungsdesign und passte die Produktionstechnik den neuen Anforderungen an. „Der Neubau in Botevgrad eröffnete die Chance, die FMD-konforme Herstellung mit State-of-the-art Technik von Beginn an unter optimalen Bedingungen zu implementieren“, betont der deutsche GE-Geschäftsführer Dr. Günter Datz. „Wir haben beschlossen, uns im Pilotprojekt gemeinsam mit unserem Produktionsdienstleister GE das notwendige Know-how frühzeitig anzueignen“, ergänzt Michael Kulmann, Leiter Operativer Einkauf bei der Wörwag Pharma GmbH. „Dadurch machen wir uns mit dem neuen Standard vertraut und haben die Möglichkeit, unser gesamtes Produktportfolio rechtzeitig auf die ab 2019 geltenden Anforderungen umzustellen.“
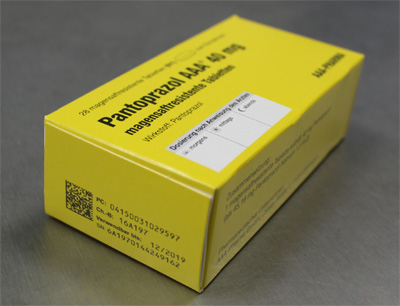
Am 5. April 2016 erfolgte die Serien-Produktion der ersten Charge von serialisierten Medikamenten: 1.000 Packungen des Magenmittels Pantoprazol 40mg liefen im Auftrag von Wörwag vom Band. Sowohl die Klebetechnik als auch die Bedruckung bewährten sich beim ersten Produktionslauf und erfüllten sämtliche Anforderungen im Rahmen des Qualitätsmanagements. Wörwag will in diesem Jahr bereits rund 150.000 FMD-konforme Sekundärverpackungen von GE herstellen lassen.
Fälschungssicher: Faltschachtel mit spezieller Klebetechnik
Die Faltschachtel für die Sekundärverpackung sollte nutzerfreundlich und wiederverschließbar sein. Die für das Öffnen präferierte Vorderseite ist mit einer nicht erkennbaren Perforierung versehen. Diese befindet sich auf der Oberseite der Verpackung, und wird von der Lasche verdeckt, die dort aufgeklebt wird. Nach dem ersten Öffnen durch Eindrücken und damit dem Einreißen entlang der Perforation kann die Verpackung auf dieser Seite wieder auf herkömmlichem Wege verschlossen werden, in dem die Lasche wieder unterhalb der Oberseite eingesteckt wird. Für den fälschungssicheren Verschluss entwickelte Baumer eine kombinierte Heiß- und Kaltklebetechnik, die einen fälschungssicheren Verschluss gewährleistet.
2D-Daten-Matrix-Code
Die Seriennummer wird auf der Rückseite aufgedruckt, und zwar in zweifacher Weise: Sie ist zum einen auf einem quadratischen, maschinenlesbaren 2D-Matrix-Code hinterlegt und zum anderen unter der Abkürzung „SN“ in vom Menschen lesbarer Schrift. Dasselbe gilt auch für den Produkt-Code, die Chargen-Nummer und das Haltbarkeitsdatum. All diese Angaben werden gemäß EU-Richtlinie ab 2019 verifiziert: das erste Mal unmittelbar nach dem Aufdrucken auf die Sekundärverpackung, das zweite Mal bei der Ausgabe am Point of Sale (Apotheke, Krankenhaus usw.). Erst nach erfolgreicher Verifizierung der gültigen Seriennummer und erfolgter Freigabe durch das IT-System darf das pharmazeutische Produkt an den Endkunden abgegeben werden.