Forschende Pharma-Unternehmen konnten 2017 die Behandlungsmöglichkeiten für Patienten mit unterschiedlichsten Krankheiten weiter verbessern. Insbesondere haben sie die Therapieoptionen durch das Arzneimittelsortiment mit 31 Medikamenten mit neuem Wirkstoff erweitert (ohne Biosimilars). Birgit Fischer, Hauptgeschäftsführerin des Verbands der forschenden Pharma-Unternehmen (vfa), kommentierte: "Mit den neuen Medikamenten kann vielen Patienten besser geholfen werden. Für einige Patienten hat die Pharmaforschung sogar erstmals eine Behandlungsmöglichkeit geschaffen."
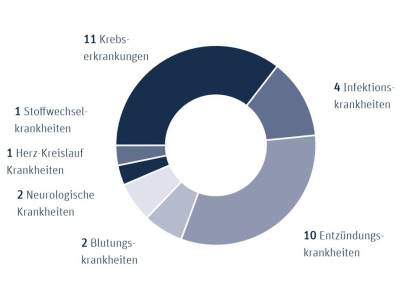
Rund ein Drittel der Medikamente mit neuem Wirkstoff (11) ist gegen verschiedene Krebserkrankungen gerichtet. Einige dieser Mittel sind immunonkologische Medikamente, die das Immunsystem der Patienten zur Tumorbekämpfung aktivieren. Andere Mittel wirken, indem sie auf die eine oder andere Weise in die Steuerung der Krebszellen eingreifen. Dazu Fischer: "Für Patienten und Ärzte ist es wichtig, dass in der Krebstherapie unterschiedliche Therapieprinzipien verfügbar sind - sei es in Kombination oder als Möglichkeit zur Anschlussbehandlung, wenn der Tumor gegen die erste Therapie resistent geworden ist. Es ist deshalb von großem Wert, dass in diesem Jahr - wie schon in den Jahren zuvor - viele Medikamente gegen unterschiedliche Krebsarten und -stadien die Versorgung erreicht haben. Schließlich erkrankt fast die Hälfte der Menschen in Deutschland im Laufe des Lebens an der einen oder anderen Form von Krebs."
Zehn weitere Medikamente mit neuem Wirkstoff dienen der Behandlung von Entzündungskrankheiten - d.h. Krankheiten, denen eine Fehlsteuerung des Immunsystems zugrunde liegt. Rheumatoide Arthritis und Asthma zählen dazu, aber auch Schuppenflechte und atopische Dermatitis (Neurodermitis). Mit zwei neuen Medikamenten können Ärzte nun eine Hepatitis C bei den meisten Patienten binnen acht statt bisher zwölf Wochen ausheilen; und dies gelingt unabhängig vom Typ der Hepatitis-C-Viren, die die Leber befallen haben.
Ein neues Antibiotikum ist gegen bestimmte multiresistente Bakterien wirksam. Zwei weitere Antibiotika durchlaufen gerade das Zulassungsverfahren. "Das zeigt," so Fischer, "dass forschende Pharma-Unternehmen auf diesem Gebiet aktiv sind und den Wettlauf gegen die Resistenzbildung aufgenommen haben. Doch weitere gemeinsame Anstrengungen von Politik, akademischer und industrieller Forschung sind nötig, damit die Medizin der Resistenzbildung bei Bakterien immer einen Schritt voraus bleibt."
Neun Medikamente mit neuem Wirkstoff sind Orphan Drugs, also Medikamente gegen seltene Erkrankungen. Unter ihnen sind die ersten Medikamente überhaupt gegen erbliche Demenz im Kindesalter (neuronale Ceroid-Lipofuszinose Typ 2), gegen das Merkelzell-Karzinom (eine Form von Hautkrebs) und gegen erbliche 5q-assoziierte spinale Muskelatrophie. Bei letzterer Krankheit verkümmern Muskeln, weil sie keine Nervenimpulse mehr erhalten. An jeder dieser Krankheiten leiden in der EU weniger als einer von 2.000 Bürgern - an der genannten Muskelatrophie beispielsweise deutschlandweit weniger als 1.300 Patienten.
Fortschritte für Patienten haben Pharma-Unternehmen auch mit Medikamenten erzielt, die bekannte Wirkstoffe in neuer Darreichungsform oder Kombination verfügbar machen. So ist ein ursprünglich für die Krebstherapie entwickelter Wirkstoff nun als Tabletten für die Behandlung von Multipler Sklerose einsetzbar. Ein Insulin senkt aufgrund einer neuen Formulierung den Blutzuckerspiegel noch schneller als bisher. Zwei weitere HIV-Medikamente sind nun auch in einer für kleine Kinder geeigneten Darreichungsform (Trinklösung bzw. Pulver) verfügbar geworden.
Nicht nur bei diesen beiden HIV-Medikamenten, sondern bei insgesamt 36 Medikamenten haben Pharma-Unternehmen 2017 das Anwendungsgebiet auf jüngere Altersgruppen ausdehnen können, nachdem sie entsprechende klinische Studien durchgeführt hatten. Zuvor hatten diese Mittel nur eine Zulassung für Erwachsene oder ältere Kinder oder Jugendliche. Diesen großen Erfolg, dass auch Minderjährige am medizinischen Fortschritt teilhaben können, leisten die forschenden Pharma-Unternehmen mit ihrem Beitrag, wie es auch die EU-Verordnung von 2007 anstrebt.